公司资讯
镍基MOF通过清除活性氧和增强血管生成促进糖尿病伤口愈合
发布日期:2024-10-08
镍基MOF通过清除活性氧和
增强血管生成促进糖尿病伤口愈合
一、摘要
慢性糖尿病伤口治疗面临挑战,因氧化应激、炎症和血管生成受损。本研究开发了镍基金属有机骨架Ni-HHTP,它抗氧化并促血管生成。Ni-HHTP能消除活性物质、保护细胞,还通过激活TGF-β1调节巨噬细胞抗炎,促进细胞迁移和血管生成。在体内,Ni-HHTP抑制炎症、促进血管生成,有效加速糖尿病伤口愈合。
二、背景
糖尿病是普遍的慢性疾病,约19-34%的患者面临慢性伤口,治疗困难,常导致严重并发症。传统疗法效果有限,迫切需要新治疗方法。糖尿病伤口愈合缓慢,受炎症、氧化应激和血管生成受损影响。高血糖和缺氧环境促进活性氧(ROS)产生,加剧炎症,减少血管生成。纳米酶,特别是金属有机骨架(MOF)材料,因模拟天然抗氧化酶、清除ROS和促血管生成而备受关注。镍(Ni)基MOF,作为NiSOD的活性中心,能消除ROS、抑制炎症,并通过激活TGF-β1和VEGF信号促进血管生成。因此,Ni基MOF为糖尿病伤口修复提供了新策略,同时消除ROS并促进血管生成。
三、Ni-HHTP的合成与表征
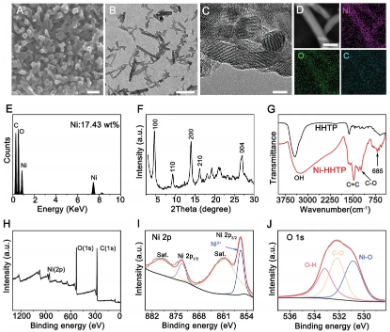
以儿茶酚配体HHTP和Ni(CH3COO)2为原料,通过水热反应合成了镍基金属有机骨架Ni-HHTP。SEM和TEM观察显示,Ni-HHTP为纳米棒状结构,具有有序多孔性,比表面积为110.22 m2/g,孔径为15.98 nm。EDS和ICP-AES分析确认Ni元素均匀分布且含量一致。XRD、FT-IR和XPS分析表明,Ni-HHTP具有特定晶体结构,Ni与HHTP成功配位形成Ni-O键,证实了Ni(II)的存在及Ni与HHTP的配合。综上,成功合成了多孔Ni-HHTP框架。
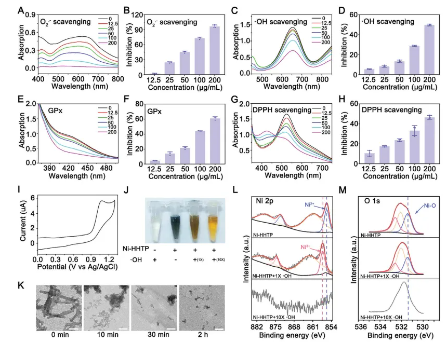
四、Ni-HHTP清除活性氧和活性氮能力
Ni-HHTP具有强大的抗氧化性能,能有效清除活性氧(ROS)和活性氮(RONS)。通过NBT、TMB和DPPH等方法评估,Ni-HHTP显示出对O2·−、·OH和H2O2的高效清除能力,以及清除RNS的活性。其抗氧化性能依赖于电子转移反应,循环伏安法证实了Ni-HHTP的强还原能力。在高浓度·OH或H2O2作用下,Ni-HHTP通过提供电子被降解,释放Ni离子,表明其自我牺牲的抗氧化机制。这种特性有助于Ni-HHTP在糖尿病伤口治疗中抑制氧化应激和促进血管生成,同时避免长期滞留的潜在毒性。
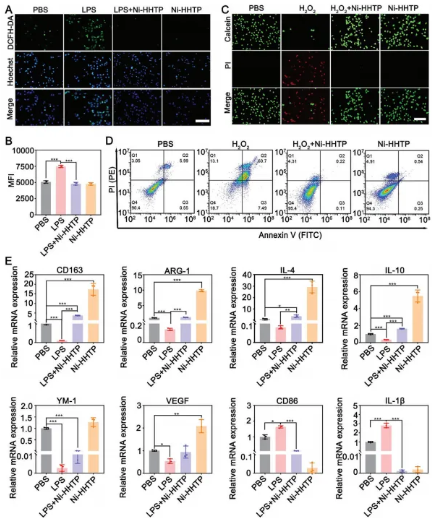
五、Ni-HHTP保护细胞免受氧化应激,并将巨噬细胞重编程为抗炎表型
Ni-HHTP具备以下三大功效:首先,它能有效清除糖尿病伤口中过量的ROS,保护细胞免受伤害,特别是在LPS刺激下,能显著降低HUVECs和NCM460细胞的ROS水平,展现出卓越的抗氧化能力;其次,Ni-HHTP能保护HUVECs细胞,防止其受到H2O2诱导的氧化应激损伤,完全恢复细胞活力;最后,Ni-HHTP还能调节糖尿病伤口中巨噬细胞的极化状态,将其从促炎表型转变为抗炎表型,通过抑制NF-KB通路激活,减少促炎细胞因子产生,增加抗炎细胞因子表达,从而打破炎症与ROS的恶性循环,加速糖尿病伤口的修复与重塑。
六、Ni-HHTP通过TGF-β1激活促进血管生成和细胞迁移
Ni-HHTP对糖尿病伤口愈合有显著促进作用。研究发现,Ni-HHTP能增强HUVECs的增殖、迁移和血管生成能力。在共培养实验中,Ni-HHTP提高了细胞活力和增殖率,显著促进了细胞迁移,使愈合率大幅提升。同时,Ni-HHTP还显著增强了HUVECs的血管化能力,形成更完整、密集的管状网络。因此,Ni-HHTP在体外实验中展现出促进创面愈合的潜力。
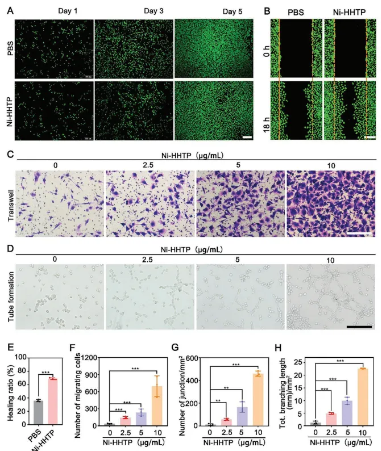
研究显示,Ni-HHTP促进血管生成的作用与其激活TGF-β1信号通路有关。在HUVECs中,Ni-HHTP能浓度依赖性地提高TGF-β1和VEGF的蛋白及mRNA水平。而使用TGF-β1受体的抑制剂后,VEGF的表达增加几乎被完全抑制,说明Ni-HHTP通过激活TGF-β1来上调VEGF。这表明Ni-HHTP促进血管生成和细胞迁移的主要机制是依赖于TGF-β1信号的激活。
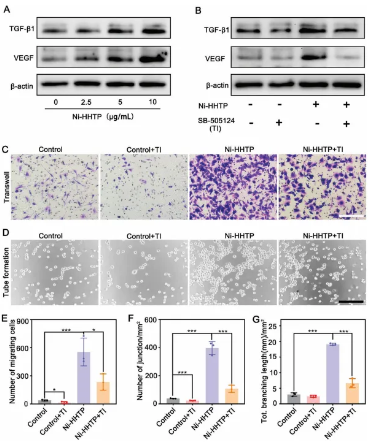
七、Ni-HHTP在体内促进糖尿病创面愈合
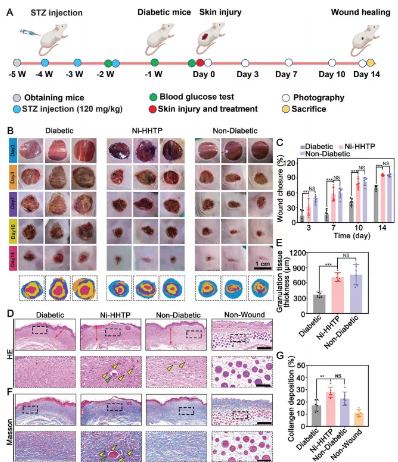
Ni-HHTP在糖尿病小鼠创面模型中展现出显著的治疗效果。与健康小鼠相比,糖尿病小鼠的创面愈合速度较慢,但Ni-HHTP治疗显著加速了糖尿病小鼠的创面愈合,达到与健康小鼠相似的水平。组织学分析显示,Ni-HHTP促进了肉芽组织增厚、上皮化完成和胶原沉积,同时增加了皮脂腺和新生血管的数量。免疫组化染色表明,Ni-HHTP上调了TGF-β1、VEGF和CD31的表达,促进了血管生成。此外,Ni-HHTP还增加了Ki-67阳性细胞数,减少了凋亡细胞,表明其促进了细胞增殖并减弱了氧化应激。综上所述,Ni-HHTP通过促进血管生成和细胞增殖,加速了糖尿病创面的愈合过程。
八、Ni-HHTP的治疗机制
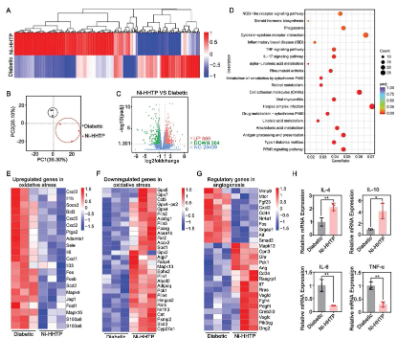
Ni-HHTP治疗糖尿病小鼠创面的转录组分析显示,其显著改变了1024个基因的表达,包括上调660个和下调364个基因,主要涉及抗氧化、抗炎和促血管生成等方面。Ni-HHTP下调了IL-17和TNF等炎症相关信号通路,上调了抗氧化基因并下调了促炎基因。同时,Ni-HHTP增加了促血管生成基因的表达,降低了不利于愈合的基因表达。qPCR和免疫组化结果进一步证实了Ni-HHTP的抗炎和促血管生成作用。总之,Ni-HHTP通过减轻氧化应激、抑制炎症和促进血管生成,显著促进了糖尿病创面的愈合。
九、总结
本研究设计了一种多功能Ni-MOF纳米酶(Ni-HHTP),能抑制氧化应激、促进血管生成,加速糖尿病慢性伤口愈合。Ni-HHTP模拟天然酶活性消除ROS,通过激活TGF-β1促进细胞迁移和血管生成,并调节巨噬细胞极化。Ni-HHTP有望成为慢性伤口愈合的纳米治疗药物,可与其他敷料结合使用。本研究展示了镍离子在消除活性物质和调节生物活性因子方面的多重生物活性。
更多服务咨询请致电:
15001394959
15555144551
17666664644
导科医药竭诚为您服务~