公司资讯
双光子显微镜技术下胶质瘤-壁细胞在体多荧光示踪小鼠模型的建立及应用
发布日期:2024-08-07

双光子显微镜技术下胶质瘤-壁细胞在体多荧光示踪小鼠模型的建立及应用
目的: 建立双光子显微镜下可视化胶质瘤、壁细胞和血管的活体自发荧光的基因小鼠模型并进行评价。
1. 材料
1.1 实验动物
种类与数量:
雄性B6.Cg-Pdgfrbtm1.1(cre/ERT2)Csln/J小鼠(简称PDGFRβ Cre+/+),10只,812周龄,体重1824g。
雌性B6.Cg-Gt(ROSA)26Sortm14(CAG-tdTomato)Hze/J小鼠(简称Rosa26-tdtomato+/+),30只,812周龄,体重1824g。
配种与繁育:
PDGFRβ Cre+/+与Rosa26-tdTomato+/+配种繁育的子代用于实验研究。
饲养环境:
SPF级屏障环境,提供不受限制的食物和水。
温度控制:22~25℃。
相对湿度控制:40%~70%。
明暗周期:12h/12h,建立昼夜节律。
1.2 细胞系
名称与来源:
GL261小鼠胶质瘤细胞系,来源于北京协和医学院细胞资源中心(PCRC)。
支原体检测:
采用DAPI染色法检测。
培养条件:
含10% FBS和1%青霉素/链霉素的RPMI-1640培养基中培养。
1.3 主要试剂与仪器
试剂:
RPMI-1640培养基、胎牛血清、麻醉剂异氟烷、FITC-dextran(HY-128868I)、CFP慢病毒、复方氯胺酮注射液、青霉素、脱毛膏、眼膏、牙科水泥乙基氰基丙烯酸酯液体(DW6993443, HAGER)、美洛昔康注射液
仪器:
手术器械、立体定位仪、Hamilton注射针筒、注射器针头-6 cm尖头31G、台式双目体视显微镜、微型手持颅钻、钻头0.5 mm HM1005-圆头、300g热玻璃珠灭菌器、Cover Slips玻璃圆片、TCS SP8 DIVE双光子共聚焦显微镜
2. 方法
2.1 基因工程小鼠的繁殖与鉴定
实验目的
通过杂交壁细胞特异性PDGFRβ-Cre+/+小鼠与Rosa26-tdTomato+/+小鼠,生成能在Tamoxifen诱导下特异性表达tdTomato红色荧光蛋白的PDGFRβ-Cre+/-; Rosa26-tdTomato+/-小鼠,用于后续实验。
实验步骤
1.小鼠杂交:
将PDGFRβ-Cre+/+小鼠与Rosa26-tdTomato+/+小鼠进行杂交。
通过Tamoxifen诱导,使得子代小鼠(PDGFRβ-Cre+/-; Rosa26-tdTomato+/-)的壁细胞特异性表达tdTomato红色荧光蛋白。
2.PCR鉴定:
使用特定引物对小鼠进行PCR鉴定,确认基因型。
PDGFRβ-Cre PCR引物:
野生型引物:
5’-AGCTTGTGGCAGTGTAGCTG-3’
突变型引物:
5’-ACATGTCCATCAGGTTTCTTGC-3’
共用引物:
5’-CCACCTTGAATGAAGTCAACAC-3’
Rosa26-tdTomato PCR引物:
野生型正向引物:
5’-AAGGGAGCTGCAGTGGAGTA-3’
野生型反向引物:
5’-CCGAAAAATCTGTGGGAAGTC-3’
突变正向引物:
5’-CTGTTTCCTGTACGGCATGG-3’
突变反向引物:
5’-GGCATTAAAAGCAGCGTATCC-3’
3.PCR反应体系:
20 μL反应体系中包含10 μL PreMix TaqTM(TaKaRa 2.0 plus dye)、2 μL鼠尾基因组DNA、1 μL 10 nmol/L前向引物和反向引物,最后加入6 μddH2O。
4.PCR程序:
· 95 ℃初始变性5 min
· 95 ℃ 30 s, 58 ℃ 30 s, 72 ℃ 30 s,共35个循环
· 72 ℃延长10 min
2.2 慢病毒感染实验
实验目的:
通过慢病毒感染GL261细胞,使其稳定表达CFP,用于后续实验。
实验步骤:
1.细胞培养:
· 制备5 × 10^4 /mL的GL261细胞悬液,并在6孔板中每孔接种2 mL。
· 37 ℃培养24 h。
2.慢病毒感染:
·在MOI = 100的条件下加入CFP慢病毒,继续培养16 h。
·中途换液保持细胞活性。
3.筛选稳定表达细胞:
感染约72 h后,加入500 μg/mL G418筛选至稳定。
2.3 器官组织形态学观察
目的:
观察C57BL/6和PDGFRβ Cre+/-;Rosa26-tdTomato+/-小鼠各器官的组织形态。
步骤:
1.取小鼠的脑、心脏、肺、肝、脾和肾等器官,固定于4%多聚甲醛中48小时。
2.脱水、透明、石蜡包埋后,进行苏木素伊红(HE)染色。
3.在光学显微镜下拍照观察。
2.4 玻璃颅窗动物模型的手术制备方法
目的:
为小鼠制备玻璃颅窗,以便进行后续实验观察。
步骤:
1.提前4周准备颅窗,使用异氟烷气体麻醉小鼠。
2.剪去头皮,磨去颅骨,挑去硬脑膜。
3.使用直径6mm的透明颅窗覆盖大脑,并用牙科水泥密封。
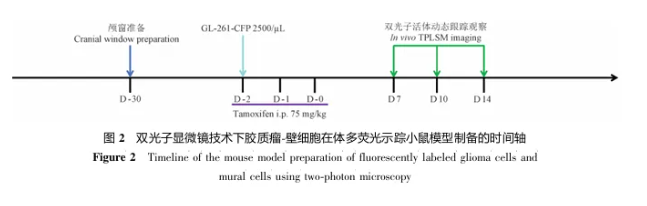
4.术后皮下 注射4剂镇痛药:每隔6 h注射一剂美洛昔康注射 液(0.1 mg/kg)。第-2、-1、0天每天腹腔注射一剂 他莫昔芬(75 mg/kg),在第3、5、7、14天使用双光子 活体动态跟踪观察,见图1。

2.5 胶质瘤活体动物模型制备方法
目的:
在小鼠脑内注射GL261-CFP细胞,制备胶质瘤活体动物模型。
步骤:
1.在已制备玻璃颅窗的小鼠上,去除玻璃片和固定环。
2.使用汉密尔顿微量注射器和针头,将GL261-CFP细胞悬液以特定速度和深度注射到小鼠脑内。
3.注射后停留片刻,然后缓慢退针。
4.清洁脑表,用牙科水泥固定玻璃圆片。
5.。术后皮下注射4针镇痛药:每隔6 h 注射一剂美洛昔康注射液(0.1 mg/kg),见图2。
2.6 双光子显微镜观察
目的:
使用双光子显微镜观察小鼠脑内的胶质瘤和血管情况。
步骤:
1.使用徕卡TCS SP8 DIVE共聚焦显微镜进行图像采集。
2.通过小鼠尾静脉注射FITC-dextran以显示脑血管。
3.设置适当的激发和发射波长,以区分不同荧光标记物(TdTomato、FITC-dextran、GL261-CFP)。
4.在麻醉状态下,以尽可能低的激光功率和气体流量进行扫描,以避免光毒性。
3. 统计学分析
通过双光子显微镜获取到的IMS文件,由 Imaris x64 9.7.2软件量化分析。计量资料均以平 均值 ± 标准误差(???? x ± s???? x)描述,采用GraphPad Prism 9.0软件进行统计分析,以P < 0.05表示差异具有显著性。
4. 结果
4.1 PDGFRβ-Cre+ /-:Rosa26-tdTomato+ /-基因鉴定
PCR扩增与凝胶电泳结果分析
1.PDGFRβ-Cre基因鉴定:
样品分析:
野生型等位基因:条带大小为272 bp。
突变型等位基因:条带大小约为320 bp。
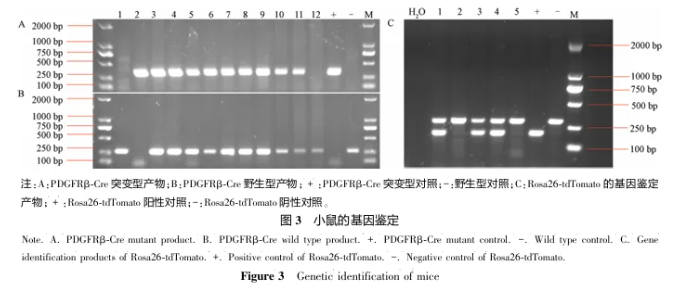
图3A ~ 3B:
1号、12号样品仅显示一条约320 bp的条带,表明它们为PDGFRβ-Cre纯合突变体(PDGFRβ-Cre-/-)。
2号样品显示两条条带,分别为272 bp和320 bp,表明它为PDGFRβ-Cre野生型与突变型的杂合体(PDGFRβ-Cre+ / +)。
3 ~ 11号样品同样显示两条条带,但具体比例可能因个体而异,表明它们均为PDGFRβ-Cre的杂合体(PDGFRβ-Cre+ /-)。
2.Rosa26-tdTomato基因鉴定:
样品分析:
突变型等位基因:条带大小约200 bp。
野生型等位基因:条带大小约为297 bp。
图3C:
1号、3号、4号样品显示两条条带,分别为200 bp和297 bp,表明它们为Rosa26-tdTomato的杂合体(Rosa26-tdTomato+ /-)。
2号、5号样品仅显示一条约297 bp的条带,表明它们为Rosa26-tdTomato的野生型纯合子(Rosa26-tdTomato-/-),即不携带tdTomato突变等位基因。
4.2 PDGFRβ-Cre+ /-:Rosa26-tdTomato+ /-小鼠表型分析
C57BL/6遗传背景的PDGFRβ + 细胞特异性
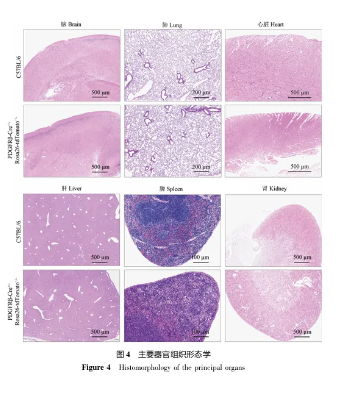
携带红色荧光的小鼠与C57BL/6小鼠的外观形态、生长速度、繁殖能力无显著性差异。HE结果显示,
PDGFRβ-Cre+ /-:Rosa26-tdTomato+ /-小鼠与C57BL/
6小鼠的脑、肺、心脏、肝、脾和肾等无显著性差异
(图4)。
4.3 PDGFRβ-Cre+ /-:Rosa26-tdTomato+ /-小鼠手术颅窗
实验准备:
1.小鼠选择:
选择8至12周龄的PDGFRβ-Cre+ /-:Rosa26-tdTomato+ /-转基因小鼠。这种小鼠模型通过Cre/LoxP系统允许在特定细胞(如PDGFRβ+细胞)中诱导表达红色荧光蛋白tdTomato,便于在显微镜下观察和追踪这些细胞。
2.手术颅窗制备:
· 颅骨开窗:
以小鼠头部的前囟(矢状缝与冠状缝的交点)为圆心,使用颅钻小心地磨去直径6mm的颅骨区域,暴露大脑皮层。
· 玻璃圆片覆盖:
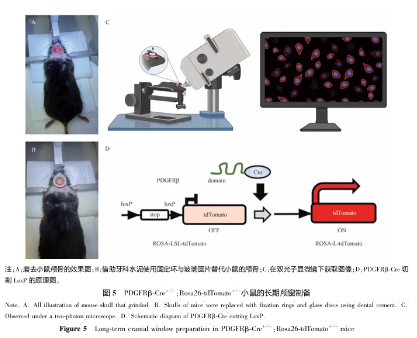
在暴露的脑表贴上一个6mm的玻璃圆片(见图5A),以保护脑组织并减少术后炎症。
· 牙科水泥固定:
围绕玻璃圆片在颅骨表面涂抹牙科水泥(见图5B),并立即安装固定环,确保固定环与颅骨之间的缝隙被水泥填满,以增强稳固性。
实验过程
1.恢复与观察准备:
手术后,小鼠需要至少4周的时间来恢复,使因手术造成的炎症消退。
2. 麻醉与注射:
使用异氟烷麻醉小鼠后,将其固定在双光子显微镜下。通过尾静脉注射200μL FITC-dextran(一种荧光标记的葡聚糖,可用于观察血管),以增强血管的可视化效果。
3.双光子显微镜图像采集(见图5C、图5D):
利用双光子显微镜采集活体小鼠大脑中的荧光图像,观察tdTomato+细胞(即PDGFRβ+细胞)的分布和动态变化。
4.4 PDGFRβ-Cre+ /-:Rosa26-tdTomato+ /-小鼠模型的活体双光子显微成像
实验准备:
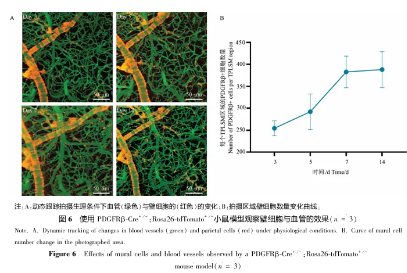
在第-30天,对三只PDGFRβ-Cre+ /-:Rosa26-tdTomato+ /-小鼠进行了颅窗手术准备。随后,在第-2天、第-1天以及第0天,每天给每只小鼠腹腔注射75 mg/kg的Tamoxifen。从第3天起,开始使用双光子显微镜进行动态的荧光成像跟踪(如图6A所示)。
实验结果:
从第3天到第7天,Tamoxifen诱导的PDGFRβ-Cre系统逐渐激活,导致tdTomato红色荧光蛋白在PDGFRβ+细胞中的表达显著增加(如图6B所示)。这一过程在大约7天后趋于稳定,表明在Tamoxifen的诱导下,所有PDGFRβ+细胞表达红色荧光蛋白所需的代谢期约为7天。
4.5 构建基于PDGFRβ-Cre+ /-:Rosa26-tdTomato+ /
小鼠的胶质瘤模型
细胞系的改造与筛选:
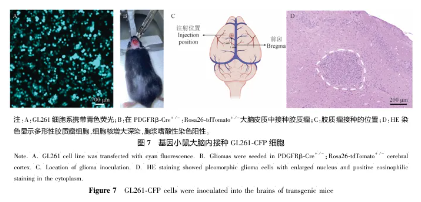
使用CFP(青色荧光蛋白)慢病毒感染GL261细胞,这一步骤使得原本不易追踪的胶质瘤细胞能够发出青蓝色荧光,便于后续实验中的观察和定位。(见图7A)
通过500 μg/mL的G418进行筛选,确保只有成功整合了CFP基因的GL261细胞能够存活并增殖,从而得到稳定的GL261-CFP细胞系。
细胞注射与定位:
将5 × 10³个GL261-CFP细胞缓慢注射到小鼠大脑皮层的特定位置(见图7B)(前囟两侧1 mm,前方2 mm处(见图7C)),这是模拟胶质瘤自然发生位置的关键步骤,有助于观察胶质瘤在体内的生长和侵袭模式。
术后处理与固定:
注射完毕后,使用生理盐水温柔地清洁脑表,以减少感染风险并保护脑组织。
贴上玻璃圆片以保护注射区域,并沿着玻璃圆片涂上牙科水泥以固定玻璃圆片和颅骨,确保后续成像过程中的稳定性。
立刻放置固定环以进一步加固结构,防止术后小鼠活动对实验造成影响。
胶质瘤模型的验证:
通过HE(苏木精-伊红)染色对胶质瘤进行组织学验证,可见多形性胶质瘤细胞、细胞核增大深染以及胞浆嗜酸性染色阳性等特征(见图7D),这些特征表明成功建立了胶质瘤模型。
4.6 胶质瘤内壁细胞及血管形态结构异常
动态追踪:
从第3天开始,通过双光子显微镜对胶质瘤生长进行动态追踪。观察到从第3天到第7天,红色荧光蛋白表达逐渐增加,第7天后趋于稳定。
胶质瘤侵袭与血管变化:
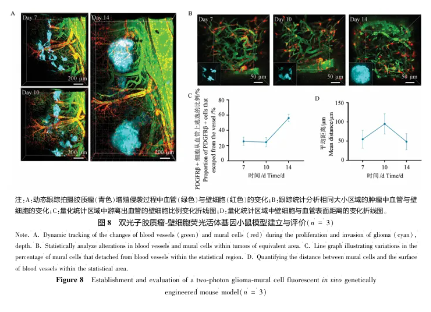
侵袭过程:第7天观察到胶质瘤开始侵袭增殖,第10天形成多发性病灶,第14天占位明显。这一过程展示了胶质瘤在体内的生长和侵袭模式。(见图8A)
血管形态变化:
随着胶质瘤的生长,血管形态发生显著变化。第7天开始,PDGFRβ+壁细胞逐渐游离出血管壁,第14天时游离比例显著增加。同时,血管脉络破碎、新生血管形成,导致血管与游离壁细胞的平均距离先上升后下降。
5.讨论
本研究通过构建壁细胞自发荧光的基因工程小鼠模型,结合双光子显微活体成像技术,实现了胶质瘤、血管及壁细胞在活体水平上的动态变化观察。双光子显微镜以其高分辨率、低光毒性和深组织穿透力,为胶质瘤与壁细胞相互作用的研究提供了高效工具。该模型不仅克服了传统成像技术的局限,还展示了胶质瘤增殖过程中血管紊乱及壁细胞形态变化的细节,为胶质瘤的发病机制、侵袭转移路径及治疗策略的研究开辟了新途径。未来,该模型有望促进胶质瘤治疗药物的研发与疗效评估,为临床治疗提供有力支持。
文章参考:马铖延,杨星九,史旭东,等. 双光子显微镜技术下胶质瘤-壁细胞在体多荧光示踪小鼠模型的建立及应用 [J]. 中国实验动物 学报, 2024, 32(6): 702-711.
更多服务咨询请致电:
15001394959
15555144551
17666664644
导科医药竭诚为您服务~