公司资讯
精原干细胞(spermatogonia stem cells, SSCs)的分离与培养-技术
发布日期:2024-08-09

精原干细胞(spermatogonia stem cells, SSCs)的分离与培养-技术
1. 精原干细胞介绍
精原干细胞(SSCs)是睾丸中最原始的“精子”,通过自我更新(即增殖,主要在A型精子)和分化和变形成为成熟的子精子,通过精卵结合形成合子(zygote)将遗传信息传递给下一代,在维持高产精子发生方面起着至关重要的作用。因此,利用SSCs研究雄性配子具有重要意义。
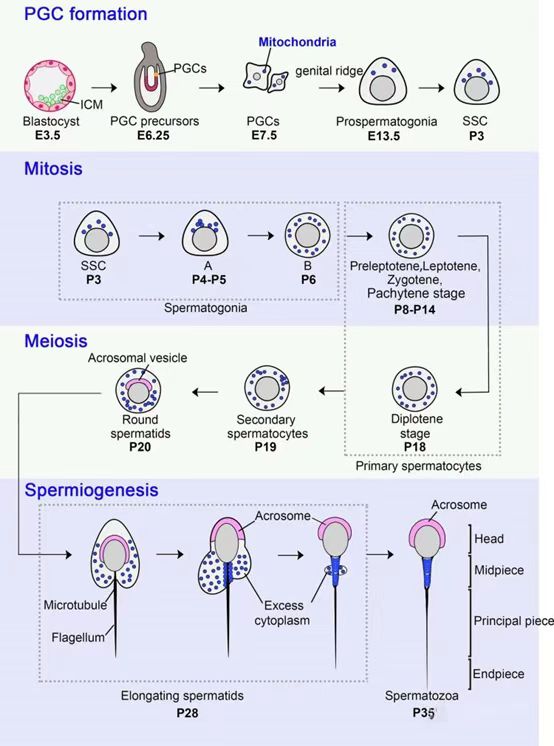
如下图所示,要准确分离和足量的SSCs选择合适时期的小鼠(mouse)是决定能否成功分离到或足量的SSCs的前提。根据以前的报道,SSCs主要在出生后第三天,新生小鼠睾丸曲细精管中存在大量(peak)的SSCs,不过一般我们在实践中会选择p4.5的小鼠进行SSCs的分离、培养、鉴定以及后续实验。
2. 实践操作
1.准备工作
1.1 器材灭菌
手术钳,剪刀,镊子,手术刀柄,吸水纸,超纯水,枪头、显微镜、恒温水浴锅、超净台等。
1.2 试剂准备
完全培养基(DMEM+5% FBS+ 2X双抗(青霉素100U/ml,链霉素0.1mg/ml)差贴使用<大部分干细胞贴壁性差甚至没有>;DMEM+1% FBS+1X双抗,培养使用);胶原酶Ⅳ(2mg/ml,使用DMEM配制),DNase(7mg/ml,PBS配制)。
2.采样与原代细胞分离
(一) SSCs分离
1. 采集完睾丸样品置于3X 双抗PBS 采样罐中(采样罐与冰袋一起放置于采样盒中),带回实验室置于4℃冰箱中(短暂放置,这是外出采样才这样处理);
2. 取出睾丸样品,使用适量3X 双抗PBS清洗组织三次,每次5分钟,然后转移至含有75%酒精的离心管中,杀菌过程中需要不断摇晃,杀菌3分钟即可(切记不能用乙醇作用时间太久,因为生殖类细胞特别容易遭受到乙醇带来的损伤),然后转移至使用3X 双抗PBS再次作用3次,每次5分钟;
3. 将睾丸组织转移至大培养皿中,在超净台中使用剪刀将白膜剥离(轻轻一扯开能很明显的区分睾丸白膜和曲细精管)。
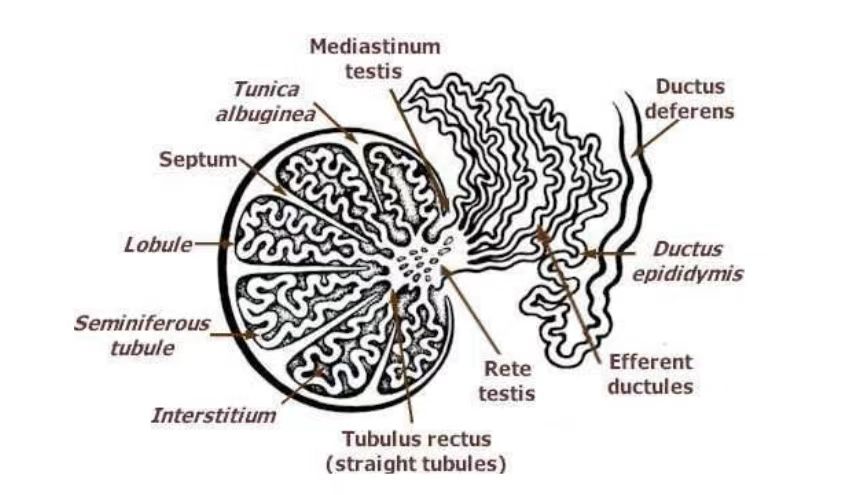
4. 将获得曲细精管转移至3X 双抗PBS中漂洗一次,然后转移至一个新的大皿中,加入少量3X 双抗PBS,剥离多余的组织;
5. 获得曲细精管使用3X 双抗PBS漂洗依稀,转移至一个新皿中,使用眼科手术钳将组织剪至1mm3左右,然后将这些组织转移至50ml离心管中,50g离心2min,吸弃上清,该步骤重复一次;
6. 加入配制好的胶原酶Ⅳ,封口胶封好管口,放入37℃摇床作用20min,消化期间,要拿出来手摇晃,避免消化不均;
7. 将上述消化后的组织,使用80g 离心2min,加入3X 双抗PBS重悬,将组织块沉降后,收集含有曲细精管上液体;
(备注:该步骤可选择加入3-5倍体积的血细胞裂解液,作用2-3min,80g离心2min)
8. 将上述收集的曲细精管液体,使用80g 2min,收集沉淀,加入适量0.25%胰酶,放在37℃水浴锅中震荡消化消化约每3分钟,即可进行镜检,以便控制消化时间,保证细胞活率;
9. 待大部分曲细精管分散成单个细胞后,加入适量血清(或等体积)终止胰酶的消化作用,收集上清,将DNase加入到沉淀中并重悬,然后使用40μm(400目)细胞筛过滤细胞;
10. 将获得的过滤液(含有细胞),450g 作用5min,弃上清,使用1-5ml完全培养基重悬,细胞计数;
11. 每2-3 *107细胞接种于10cm培养皿中,然后加入8-10ml完全培养基,差异化贴壁3次(1h-2h-过夜)(最先贴下去的是支持细胞-少量的管周肌样细胞-极极少量的间质细胞);
12. 收集差异化贴壁过夜后的细胞,450g 作用5min,弃上清,加入1ml培养基重悬沉淀,然后细胞计数接种(1.5*105/6 well 或6*104/12 well)
3. SSCs传代
1. 原代精原干细胞每2-3d换一次培养基,7d左右进行一次传代;
2. 将培养基吸弃,加入预热0.05%胰酶(可以先用低浓度消化),放入培养箱(37℃,5% CO2)中消化1-2 min(消化过程中需要不断观察,避免消化过度);
3. 加入等体积的完全培养基,终止胰酶的消化,轻轻吹打培养皿,制备细胞悬液;300g,离心5min;
4.将上清吸弃,获得细胞沉淀并重悬,调整细胞密度,将细胞悬液种至含有饲养层(基质胶)包被的培养皿中,于培养箱中培养。
更多服务咨询请致电:
15001394959
15555144551
17666664644
导科医药竭诚为您服务~